中国の臨床研究開発は過去5 ~ 10年で急速に伸びている。しかし、大量に開発された薬はすべて同質化競争に陥っており、この局面は続くことは難しいだろう。ますます多くの企業がこの問題に焦点を当て、解決しようとするにつれて、中国の臨床試験は粗放型成長から高品質成長への転換が期待されている。
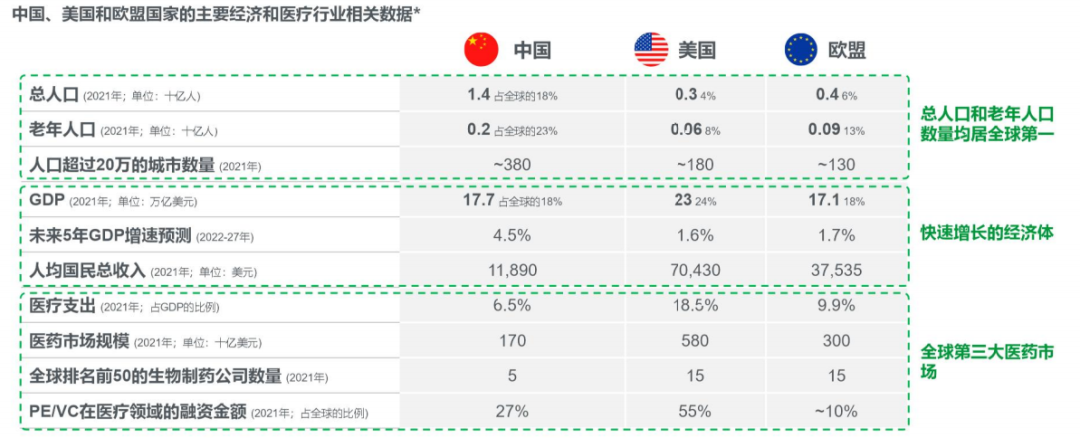
1中国臨床試験の基本概況中国、米国、EU諸国の主要経済と医療健康業界に関する指標を見ると、中国の医療市場は強力な成長基盤を備えている。
中国は現在、最大の患者集団を持ち続け、医薬支出を負担する能力が増強されている。しかし同時に、中国市場も薬品価格のストレス、患者意識の欠如、最先端イノベーションの不足など多くの挑戦に直面している。
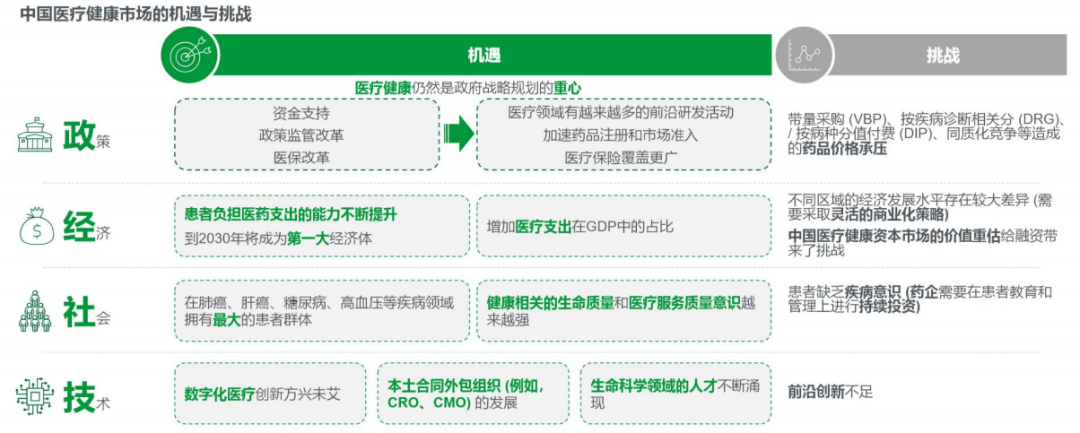
政策の好調、革新的な薬物の研究開発の加速、研究開発への投入の持続的な増加などの要素の推進の下で、中国の臨床試験は過去5年間で急速に増加した。
革新的な薬物開発の加速:中国の早期臨床試験は力強く成長し、革新能力は急速に国際的なリードレベルを追いかけ、新薬物の開発は中国の臨床試験数の力強い成長を大きく推進した。
2016-2021年の間、早期試験の伸び率はより速く、I期とII期試験の年複合伸び率はそれぞれ29%と47%だった。
いくつかの革新的な分野では、中国はすでにCAR-TやADCなどの世界的な臨床開発のリーダーとなっている。
2.中国の臨床試験の将来の発展傾向
多くの課題に直面しているが、中国の医療健康市場の基礎は依然としてしっかりしており、中国の臨床試験の将来の質の高い成長を支えることが期待されている。この背景には、4つの戦略的トレンドが予測されます。
1)より革新的で差別化された治療法の開発:近年、中国の薬企業は革新の面で一定の進展を遂げた、しかし、多くの薬物開発は人気のあるターゲット(例えばPD−1、EGFR)に集中し、さらに同質化競争を引き起こす。薬企業が新しい薬物モデル、技術プラットフォーム、標的に注目し始めるにつれて、より多くの革新的で差別化された治療法が誕生すると予想されている。同時に、同質化競争に対応するために、薬企業たちも二重特異性抗体、抗体カップリング薬、細胞/遺伝子療法など、より多くの新興薬物モデルに注目しており、中国市場もより多元化するだろう。
2)腫瘍は過去数年間、中国の臨床開発で最も人気のある治療分野となっている。将来、薬企業は医薬開発を行う際により全面的に考慮することが多く、製品の商業的魅力はその中の1つの極めて重要な考慮要素となるだろう。その他の考慮事項には、ROI(投資収益率)、企業独自のリソースの提供、外部協力の実現可能性も含まれます。
より多くの革新的な製品の発売に伴い、市場の注目ポイントは従来の「迅速な製品の成功の推進」から「ビジネスの魅力」に変わった。それは、製品がますます同質化する競争の下で最終的に成功するかどうかを直接決定するからだ。
さらに重要なのは、ビジネスにとって魅力的な製品は、会社の将来の持続的な発展をよりよく保障することができます。
→持続可能な市場収益は未来の革新的な研究開発に使用される、
→将来の外部投資を誘致するための強力な評価、
→バイオテクノロジー会社からバイオ製薬会社への転換に成功した。

3)よりインテリジェント化された臨床試験ツールの応用:臨床試験の複雑さの向上に伴い、インテリジェント化とデジタル化ツールの需要は日増しに増加している。電子化データ収集システム(EDC)、臨床試験プロジェクト管理システム(CTMS)、臨床試験マスタードキュメント管理システム(eTMF)、薬物警戒システム(PVS)などの技術はすでに中国の臨床試験で広く応用されている。将来の臨床試験では、インテリジェント化とデジタル化ツールが不可欠になり、革命的な影響さえもたらすと信じられている。
遠隔臨床試験はすでに話題になっており、最近では規制当局の注目も集まっている。遠隔臨床試験の将来の発展は駆動力と抵抗力に直面し、臨床試験の効率を高めることが主な駆動力であり、政策の不確実性が主な抵抗である。
4)双方向で中国のバイオ製薬会社に赴くグローバル化及び多国籍製薬企業の中国での研究開発戦略の進化:グローバル化は中国のバイオ製薬会社にとってますます重要であり、海外臨床試験を成功させるために、目的地の国を慎重に選択し、現地で研究開発団チームを設立し、現地の監督管理機関と積極的にコミュニケーションするなどの要素がますます多くの製薬企業に考慮されている;本土の革新薬は国際市場の認可を得ており、そのグローバル権益は海外企業に買収されつつある。
その中で、リードする多国籍薬企業は積極的に中国の革新的な資産の導入を許可しており、多国籍薬企業は中国研究開発センターの設立から中国パートナーセンターまたは孵化センターの設立に移り、中国本土の生物製薬会社との協力を促進している。
おすすめ
- 2024-03-18
- 国家医療保険局の対応:インターネット医療の革新を大いに支持し、新技術、新設備の臨床進出を加速させる 2023-12-21
- 2023-11-09
- 2023-11-03

